認知症を調べる為に、RI薬剤を利用した核医学検査が盛んになってきている。現在、治験で行われている放射性薬剤の中に、PBB3、PIBというものがある。
RI薬剤とは、放射線を出す物質である放射性同位体(Radio Isotope:RI)を体内にとりこませて、身体の器官の以上が無いかを調べることが出来る薬剤である。体内にある物質と化学的性質の近いものを使用し、μg程度の微量なRIを投与する為、身体への副作用はほぼ無いに等しい。
アルツハイマー病の患者の脳には、細胞の内外に特徴的なタンパク質が沈着することが知られている。これらは、細胞外アミロイド沈着(老人斑)や、細胞内リン酸化タウタンパク沈着(神経原線維変化)として見られる。このような認知症に特有のタンパク沈着を画像化することによって、認知症か否かを調べる研究が行われている。
RI薬剤とは、放射線を出す物質である放射性同位体(Radio Isotope:RI)を体内にとりこませて、身体の器官の以上が無いかを調べることが出来る薬剤である。体内にある物質と化学的性質の近いものを使用し、μg程度の微量なRIを投与する為、身体への副作用はほぼ無いに等しい。
アルツハイマー病の患者の脳には、細胞の内外に特徴的なタンパク質が沈着することが知られている。これらは、細胞外アミロイド沈着(老人斑)や、細胞内リン酸化タウタンパク沈着(神経原線維変化)として見られる。このような認知症に特有のタンパク沈着を画像化することによって、認知症か否かを調べる研究が行われている。
via www.nirs.go.jp
健常者や認知にやや障害がある軽度認知障害(MCI)でもアミロイドが見られるが、逆にアミロイドが見られない(陰性像)の場合は、ほぼアルツハイマー病を否定出来る。従って、従来アルツハイマー病と鑑別が困難だった認知症との鑑別と病態理解につながると考えられる。
アミロイドはタンパク質がペプチド結合部で連結し、βシートと呼ばれる二次構造を形成し、凝集したもの。(βアミロイドとも呼ばれる。)
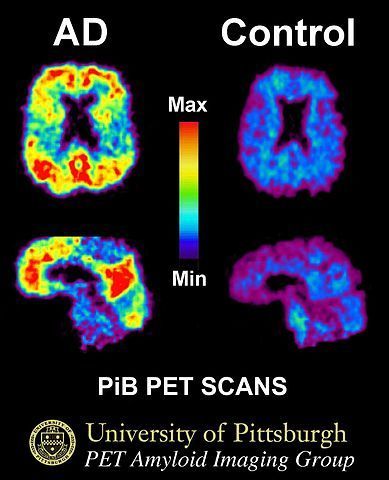
このアミロイドを画像化する薬剤として、ピッツバーグ大学で開発された11C-PIB(Pittsburgh compound-B)が感度・特異度とも優れ、標準的診断薬として用いられている。
アミロイドはタンパク質がペプチド結合部で連結し、βシートと呼ばれる二次構造を形成し、凝集したもの。(βアミロイドとも呼ばれる。)
このアミロイドを画像化する薬剤として、ピッツバーグ大学で開発された11C-PIB(Pittsburgh compound-B)が感度・特異度とも優れ、標準的診断薬として用いられている。
via en.wikipedia.org
最近の研究では、認知症につながる神経細胞死に密接に関わるのは神経の外に蓄積するβアミロイドではなく、神経細胞の内部に蓄積するタウタンパクであると考えられている。
そこで、タウ病変を画像化することでβアミロイドの画像化では十分評価できなかったアルツハイマー病の病勢評価や根本的治療法の開発が可能になると考えられ、生体脳でタウ病変に結合するPET薬剤の開発が国内で行われている。
その薬剤の1つが11C-PBB(Pyridinyl-Butadienyl-Benzothiazole)である。
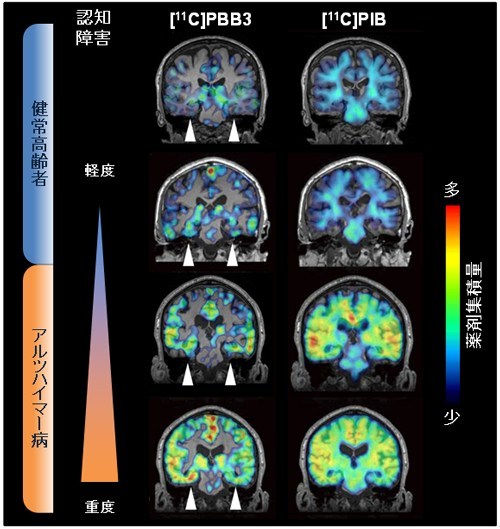
放射線医学研究所では、2013年にPBB3により、アルツハイマー病の脳内のタウ蓄積を明瞭に画像化することに成功した。また、PBB3はアルツハイマー病だけでなく、他の認知症で形成されるタウ病変も描出し、神経細胞の脱落を鋭敏に検出できる手段として認知症診断に広く応用できることも明らかになった。
そこで、タウ病変を画像化することでβアミロイドの画像化では十分評価できなかったアルツハイマー病の病勢評価や根本的治療法の開発が可能になると考えられ、生体脳でタウ病変に結合するPET薬剤の開発が国内で行われている。
その薬剤の1つが11C-PBB(Pyridinyl-Butadienyl-Benzothiazole)である。
放射線医学研究所では、2013年にPBB3により、アルツハイマー病の脳内のタウ蓄積を明瞭に画像化することに成功した。また、PBB3はアルツハイマー病だけでなく、他の認知症で形成されるタウ病変も描出し、神経細胞の脱落を鋭敏に検出できる手段として認知症診断に広く応用できることも明らかになった。
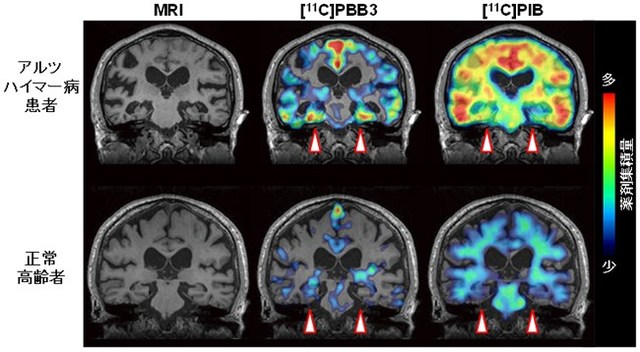
以下が比較対象の画像である。(放射線医学研究所HPより抜粋)
via www.nirs.go.jp
via www.nirs.go.jp
画像では右側頭葉の萎縮が著明であるが、タウタンパクの沈着箇所を調べることで、萎縮前に何らかの治療を行うことが今後可能になるかも知れない。
また、タウ病変は脳内の狭い領域から始まって広がっていくことが分かってきたことから、物忘れや感情の変化といった認知症の症状が脳内のどのような神経回路の異常で起こってくるのか、さらにどのような条件で症状の進展が止められるかといった研究に極めて重要な手がかりを与えてくれると期待されている。
また、タウ病変は脳内の狭い領域から始まって広がっていくことが分かってきたことから、物忘れや感情の変化といった認知症の症状が脳内のどのような神経回路の異常で起こってくるのか、さらにどのような条件で症状の進展が止められるかといった研究に極めて重要な手がかりを与えてくれると期待されている。
<参考資料>
認知症で神経細胞死を引き起こす異常タンパク質の生体での可視化に世界で初めて成功―タウ※1タンパク質病変を画像化するPET※2薬剤を開発―(放射線医学研究所HP 2013/9/19)
佐々木雅之、桑原康雄編(2015)『核医学検査技術学 改訂3版』南山堂
認知症で神経細胞死を引き起こす異常タンパク質の生体での可視化に世界で初めて成功―タウ※1タンパク質病変を画像化するPET※2薬剤を開発―(放射線医学研究所HP 2013/9/19)
佐々木雅之、桑原康雄編(2015)『核医学検査技術学 改訂3版』南山堂
10 件


 エルピクセル編集部
エルピクセル編集部





